Faktenwissen
Was
bedeutet Homologie in der Evolution? Ein Beispiel aus der Forschung
Wie Modularität von Proteinen die Evolution erleichtert
Den Begriff Homologie
kann
man treffend mit "phylogenetischer
Ursprungsgleichheit"
übersetzen. Das heißt, homologe Merkmale
verschiedener
Arten stammen von einem gemeinsamen Vorfahren ab. Obwohl in
vielen
Fällen eindeutig, ist Homologie nicht immer einfach zu
ermitteln;
je nach Faktenlage können sich Verwandtschafts-Hypothesen auch
ändern. Doch das genaue Prozedere braucht uns hier nicht zu
kümmern.
Einander homolog sein können
Gene,
Enzyme,
anatomische
Merkmale wie Organe oder Knochen sowie Verhaltensweisen. So sind
mittlerweile viele Gen- und Proteinfamilien bekannt, deren
Mitglieder einander homolog sind, also auf einen gemeinsamen Urahn (das
"Ur-Gen"
der betreffenden Familie) zurückgehen.
Bekannte Beispiele sind das bei fast allen Organismen vorkommende
Enzym Cytochrom
C, mit dessen Hilfe einer der ersten
Molekularstammbäume
errechnet wurde, sowie die bei Wirbeltieren vorkommenden Globine, die
dem
Transport oder der Speicherung von Sauerstoff dienen.
Ein klassisches
Beispiel für anatomische Strukturen sind die Homologien
zwischen
Teilen des Wirbeltierskeletts, so zum Beispiel zwischen den
Flügeln
der
Fledermäuse, den Vorderhufen der Pferde, den Flossen der Wale
und
unseren Armen. Auch bei Verhaltensweisen können Homologien
ausgemacht werden. So ist unser menschliches Lachen dem sogenannten
"Spielgesicht"
der Primaten homolog, und der Klammerreflex von menschlichen
Neugeborenen, bei dem nacheinander alle Finger in die charakteristische
Greifposition einlaufen, dem Klammerreflex von Affenbabys, mit dem sich
die Tiere im Fell der Mutter festhalten.
Diese und
unzählige andere Beispiele scheinen zu zeigen, dass der
Begriff "Homologie" ein eindeutiger ist: Zwei
betrachtete
Merkmale sind entweder ursprungsgleich oder sie sind es nicht
- doch so einfach liegen die Dinge nicht! Schon
auf genetischer
Ebene wird es kompliziert: Gene könne, etwa durch
eine "Translokation",
fremde DNA-Anteile aufnehmen. Die ursprüngliche und die neue
Gen-Variante sind dann nur noch
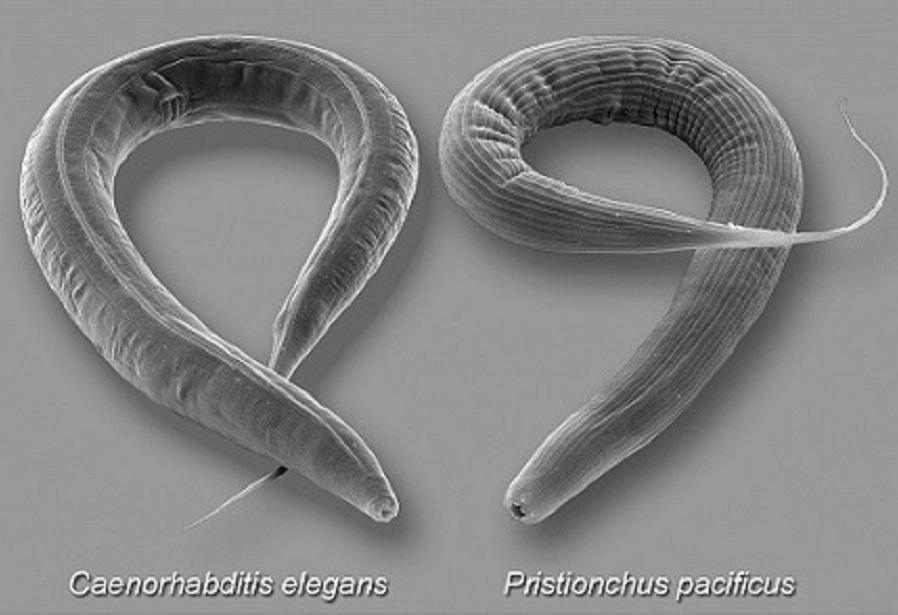
zum Teil homolog. Aber es geht noch komplexer: Die Arbeitsgruppe um den
Evolutionsbiologen Ralf SOMMER konnte zeigen, dass bei verschiedenen
Nematoden wie den Modell-Organismen Caenorhabditis elegans und
Pristionchus
pacificus die Bildung der Vulva von verschiedenen
Signalwegen getriggert wird (WANG & SOMMER 2011). Das
Organ hingegen, der
Eiablageapparat,
blieb in der äußeren Form bei beiden
Tieren gleich.
Die Evolution scheint mit anderen Worten "die vorhandenen Signalwege
fast wie ein Baukastensystem zu nutzen: Eine Signalkette kann wie bei P.
pacificus an einer neuen Stelle angekoppelt und in einem
neuen Zusammenhang genutzt werden" (MPI
Tübingen). Ein solcher developmental
systems drift ist
erwartungsgemäß selten, kommt
aber vor. Und im
Falle der Nematoden waren, wie genetische Analysen zeigen, offenbar
auch keine grundlegenden genetischen Änderungen bzw. lange,
umfassenden Mutationsserien dafür notwendig. Der modulare
Aufbau der Proteine scheint der
Evolution Freiräume zu schaffen und die regulatorischen
Entwicklungs-Mechanismen stark verändern zu können,
während die
Strukturen der Organe wie auch der Signalketten
häufig über lange Zeiten hochkonserviert bleiben.
In solch einem
Fall
muss man die anatomischen Strukturen also als einander homolog
betrachten,
die
triggernden Signalwege hingegen als analog. Überwiegend aber
kommt
der umgekehrte Fall vor. Die morphologischen und anatomischen
Strukturen Augen der Wirbeltiere und der Komplexaugen der Insekten etwa
haben unterschiedlichen Ursprung, sind als unabhängig
voneinander
(konvergent) entstanden. Die Signalwege sind jedoch einander homolog,
haben also den gleichen evolutionären Ursprung. In der
Evolution
kam es im Wesentlichen nur darauf an, bei Insekten und Wirbeltieren
sukzessive unterschiedliche Strukturgene in die Signalwege
"einzuschalten".
Quelle
MPI Tübingen: Wie der modulare Aufbau der Proteine die
Evolution fördert.
https://www.mpg.de/forschung/signalwege-evolution
WANG, X. & SOMMER, R. J. (2011) Antagonism of LIN-17/Frizzled
and LIN-18/Ryk in Nematode Vulva Induction Reveals Evolutionary
Alterations in Core Developmental Pathways.
PLoS Biology,
https://doi.org/10.1371/journal.pbio.1001110
Autor: Andreas
Beyer

© AG
Evolutionsbiologie des VdBiol.
11.11.2019


