|
Allgemeines
Publikationen
|
Druck-Version
Faktenwissen
Wie tierische Zellen aneinander haften
Evolution der Zelladhäsion bei Vielzellern
Multizelluläre Organismen - also die komplexer gebauten Tiere (Metazoen) und Pflanzen - brauchen, um funktionieren zu können, Eigenschaften, welche von Einzellern nicht benötigt werden. Zu nennen wären beispielsweise:
- Zell-Zell Kommunikation (über größere Zellverbände oder über den ganzen Körper hinweg auf (bio-) chemischem Wege über Hormone oder gezielt von einer Zelle zur nächsten über Neurotransmitter, also auf nervösem Wege).
- Zelldifferenzierung: Der Organismus besteht aus etlichen bis hunderten verschiedenen Zelltypen; diese müssen koordiniert und unter mehr oder weniger strikter Regulation aus undifferenzierten Vorläuferzellen gebildet werden.
- Zelladhäsion: Die Zellen des Organismus müssen, damit er eine definierte Gestalt ausbilden kann, auf bestimmte Weise aneinander haften.
Damit Mehrzeller entstehen konnten, mussten also diese Vorbedingungen erfüllt sein. Nun muss man sich fragen, was dem gemeinsamen Vorfahren der Metazoen, einem einzelligen Lebewesen, Eigenschaften wie interzelluläre Kommunikation oder Zelladhäsion genützt haben sollen. Kann man sich tatsächlich vorstellen, dass diese Eigenschaften in einem einzelligen Lebewesen evolvierten? Die Alternative, nämlich die gleichzeitige, mehr oder weniger sprunghafte Entstehung all dieser Eigenschaften und Fähigkeiten zusammen mit der Mehrzelligkeit, ist derart unwahrscheinlich, dass man an diese Möglichkeit keinen Gedanken zu verschwenden braucht.
Was also ist des Rätsels Lösung? Wie so oft so zeigt sich auch hier, dass die menschliche Fantasie unzureichend ist, wenn es darum geht, historische Abläufe allein mit Hilfe der Vorstellungskraft zu rekonstruieren. Man kann sich mit seinem "gesunden Menschenverstand" kaum von der Idee lösen, dass all diese Elemente erstmals in einem Einzeller vorhanden gewesen sein mussten (der davon allerdings nicht profitieren konnte), bevor sich die Metazoen überhaupt entwickelten konnten. Doch hier liegt ein fundamentaler Irrtum vor, und zwar bezüglich der Vorstellung, dass es "die Einzelligkeit" und "die Vielzelligkeit" gäbe, dass oben benannte Eigenschaften für Einzeller grundsätzlich nutzlos seien und dass es keine Organisationsformen zwischen Ein- und Mehrzelligkeit geben könne.
Glücklicherweise hat uns die Natur an einigen Stellen Hinweise über die Entwicklung hinterlassen: Viele Einzeller kommunizieren über sog. Pheromone; etliche wechseln in ihrem Lebenszyklus zwischen ein- und mehrzelligen Phasen (z.B. bildet Dictyostelium discoideum unter Hungerbedingungen vielzellige Fruchtkörper). Schwämme haben keine echten Gewebe und erst recht keine Nervenzellen, aber die Zellen kommunizieren bereits auf eine Art und Weise, wie es die Nervenzellen höherer Tiere tun (natürlich weitaus einfacher).
Nun haben Sebé-Pedrós et al. (2010) eine Untersuchung veröffentlicht, die sich mit der Evolution der Zelladhäsion und der damit verbundenen Kommunikationsprozesse befasst. Tierische Zellen heften sich mithilfe unterschiedlicher Proteinsysteme an; das wichtigste ist der Integrin-Adhäsionskomplex (Abb. 1).
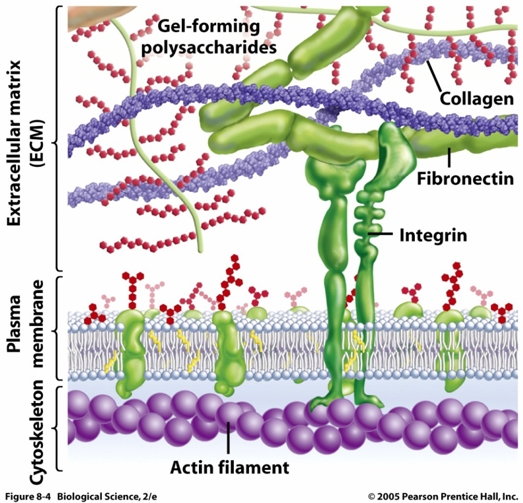
Abb. 1: Integrine sind sog heterodime (= aus zwei veschiedenen Untereinheiten aufgebaute) Transmembranproteine, d.h. sie durchqueren die Zellmembran. Sie bestehen aus einer alpha- und einer beta-Untereinheit. Ihre Hauptaufgabe besteht darin, das Zellskelett ("Zytoskelett", aus Aktin bestehend, in der Abb. unten) mit der Extrazellularmatrix, also den Stützstrukturen zwischen den Zellen zu verbinden. Dieser Kontakt erfolgt indirekt, d.h. es existieren inner- und außerhalb der Zelle noch weitere Brückenmoleküle wie alpha-Actinin, Talin (an Integrin-beta bindend) sowie Paxillin und Vinculin (ihrerseits an Talin und alpha-Actinin bindend). Der Integrin-Komplex dient auch der Nachrichtenübermittlung. Quelle: http://www.uic.edu/classes/bios/bios100/f06pm/integrin.jpg
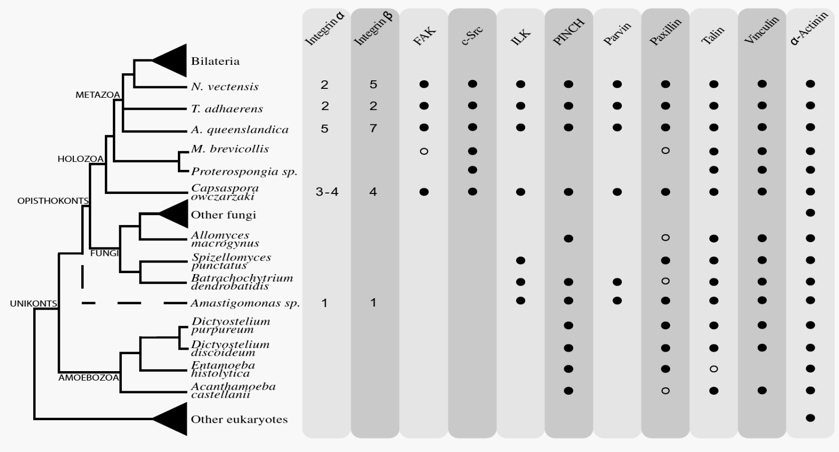
Die Autoren verglichen die mittlerweile komplett sequenzierten Genome etlicher Ein- und Mehrzeller und suchten nach Genen für Integrin und solche Proteine, die mit Integrin wechselwirken. Das Ergebnis war unerwartet, aber bei näherer Betrachtung alles andere als überraschend: Die Präsenz des Integrin-Systems lässt sich bis weit in das Reich der Einzeller zurückverfolgen (Abb.2).
Abb.2: Anwesenheit unterschiedlicher Komponenten des Integrin-Komplexes in verschiedenen eukaryontischen Gruppen. Schematischer Stammbaum der Eukaryoten (mit besonderem Augenmerk auf den Zweig der Animalia, Tiere). Dargestellt sind die verschiedenen Komponenten des Integrin Adhäsions-Komplexes. Spalte 1+2: Anzahl der Integrin-Homologen. Schwarzer Punkt: Homologe (mit deutlicher Sequenzähnlichkeit) klar identifizierbar. Weißer Punkt: Kandidaten für Homologe mit geringerer Ähnlichkeit. Kein Punkt: Gen nicht vorhanden. Die meisten Elemente des Zellskeletts (Myosin, Aktin, Tubiulin etc.) sind nicht aufgeführt - sie sind bei praktisch allen Eukaryonten vorhanden. Aus: SEBÉ-PEDRÓS et al. (2010).
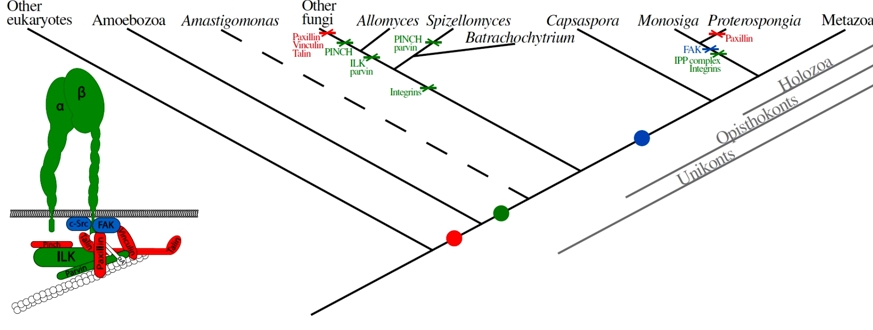
Ausgehend von diesen Befunden lässt sich ein Szenario rekonstruieren, welches die Evolution des Integrin-Komplexes beschreibt (Abb.3). Eine der wichtigsten Lehren, die man (beileibe nicht nur aus diesem Fall) ziehen kann, ist die folgende Erkenntnis: Komplizierte, biologische Systeme sind in der Tat irreduzibel komplex. Wer jedoch daraus schließt, dass sie in einem Schritt entstanden (ergo: designt) worden seien, begeht einen Denkfehler. Bei genauer Betrachtung wird man fast immer Systeme finden, die einfacher gebaut sind und/oder bei denen Komponenten fehlen oder zusätzliche Komponenten vorhanden sind. Diese Systeme funktionieren ebenfalls, möglicherweise weniger effizient oder differenziert, fast immer in einem mehr oder weniger ähnlichen oder auch abgewandelten funktionellen Kontext - gerade so, wie man es aus evolutionstheoretischer Perspektive erwartet.
Abb.3: Modell der Evolution des Integrin-Adhäsions- und des Integrin-signalkomplexes. Links: Der "kanonische", eukaryontische Integrin-Komplex. Die Farben bezeichnen die drei Haupt-Schritte der Entwicklung, rechts im Kladogramm entsprechend markiert. Punkte bezeichnen die Entstehung, Kreuze den Verlust der betreffenden Anteile. Der Zweig, der zu Amastigomonas führt, ist gestrichelt, weil seine phylogenetische Position noch nicht ganz klar ist.
Interessanterweise ist die Fähigkeit zur Adhäsion an verschiedene Oberflächen auch bei Bakterien eine sehr weit verbreitete Eigenschaft. Tatsächlich gibt es so gut wie keine Bakterienarten, die sich nicht mittels Adhäsine an Oberflächen anheften können (AN/FRIEDMAN 2000; DUNNE 2002). Während zur einfachen Erst-Adhäsion simple elektrostatische Wechselwirkungen und Van-der-Waals-Bindungskräfte ausreichen (RAZATOS et al. 1998), gibt es für eine feste Adhäsion ein immens breites Spektrum an Adhäsions-Molekülen (PIZARRO-CERDÁ/COSSART 2006; SOTO et al. 1999). Eine der immer wiederkehrenden und für funktionelle Adhäsion wichtige Protein-Domäne (Motiv) ist das so genannte "parallele beta-Faltblatt" (in Form von sog. beta-sheets oder beta-barrels, wie man diese Elemente in der Strukturbiologie nennt; Abb. 4 und 5) (NIEMANN et al. 2004). Derart gebaute Struktur-Motive vermitteln die Adhäsion an andere Proteine und sind oft gekennzeichnet durch häufige Wiederholung der Aminosäuren Leucin, Isoleucin und Valin (leucin-rich repeats) (KOBE/KAJAVA 2001). Dieses Motiv ist interessanterweise keinesfalls spezifisch für Adhäsine, sondern findet sich auch in vielen anderen Enzymen wie auch integralen Proteinen der äußeren Zellmembran (NIEMANN et al. 2004, JENKINS/PICKERSGILL 2001). Festzuhalten ist, dass Bakterien wie eukaryote Einzeller die Fähigkeit zur Adhäsion schrittweise entwickelten, ohne dass diese Eigenschaft zunächst etwas mit Vielzelligkeit zu tun hatte.
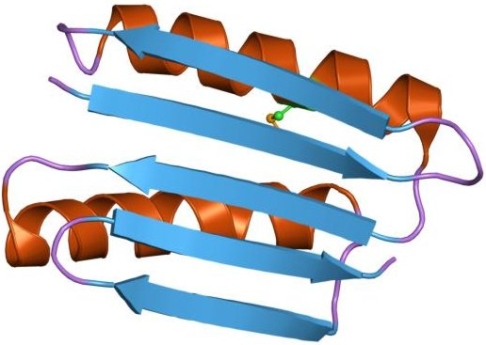
Abb.4: Schemazeichnung eines Strukturblocks in einem Protein mit ß-Faltblatt.
Der durchgehende "Faden" stellt die Aminosäurekette dar, in den braunen "Schrauben" ist er zur sog. alpha-Helices aufgerollt. Die blauen Pfeile stellen "beta-strands" dar, die sich zu einem beta-Faltblatt zusammen gelagert haben.
http://upload.wikimedia.org/wikipedia/commons/2/21/PDB_1qys_EBI.jpg
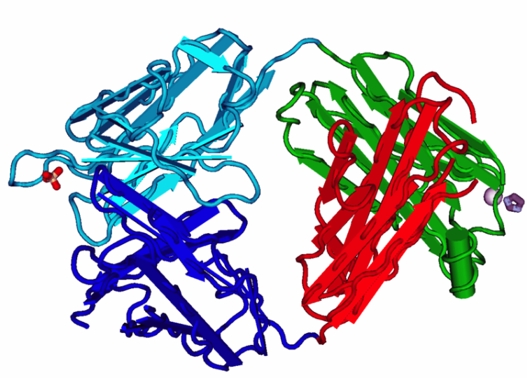
Abb.5: FAB Fragment des IGG aus beta-folds. Die meisten Proteine beinhalten sowohl alpha-Helices als auch beta-Faltblätter. Die Antikörper hingegen - hier ein die Struktur des sog. FAB-Fragments des Antikörpers Immunglobulin G (IGG) dargestellt - sind ausschließlich aus beta-Faltblättern und kurzen, verbindenden Schliefen aufgebaut. Quelle: http://upload.wikimedia.org/wikipedia/commons/.../800px-1MRC_Igg_Jel_103_Fab_Fragment.png
So weit verbreitet und simpel die "parallele beta-Faltblatt"-Struktur auch ist, so vielfältig ist dessen Evolution (JENKINS/PICKERSGILL 2001). Eine derart einfache Struktur ist mit Sicherheit viele Male parallel evolviert; hinzu kommen Gen- und Domänenduplikationen (JENKINS/PICKERSGILL 2001) sowie horizontaler Gentransfer.
Fazit
Es zeigt sich immer wieder, dass die meisten Systeme, die bei mehrzelligen Tieren wichtige Aufgaben erfüllen, bei einzelligen Vorfahrenarten bereits in ähnlicher, zumeist präadaptierter Form vorhanden waren - wie nicht anders zu erwarten in einfacherer und bisweilen rudimentärer Form. Die Evolution verlief mosaikartig und Schritt für Schritt: Die Systeme etablierten sich nach und nach und wurden in der einen Abstammungslinie durch Gen-Verdopplung und Rekrutierung anderer Gene schrittweise komplexer, während sie in anderen Linien durch Genverlust einfacher wurden oder gar vollständig verschwanden. In solchen Organismen, in denen ein System aufgrund seiner Beschaffenheit neue Optionen eröffnet, standen der Evolution neue Wege offen, z.B. der Weg in die Mehrzelligkeit.
Literatur
AN, Y.H./ FRIEDMAN, R.J. (2000) Handbook of Bacterial Adhesion: Principles, Methods, and Applications. Humana Press.
DUNNE, W.M. Jr (2002) Bacterial Adhesion: Seen Any Good Biofilms Lately? Clin Microbiol Rev 15, 155-166.
JENKINS, J./ PICKERSGILL, R. (2001) The architecture of parallel -helices and related folds. Progress in Biophysics and Molecular Biology 77, 111-175.
KOBE, B./ KAJAVA, A.V. (2001) The leucine-rich repeat as a protein recognition motif. Current Opinion in Structural Biology 11, 725-732.
NIEMANN, H.H./ SCHUBERT, W.-D. et al. (2004) Adhesins and invasins of pathogenic bacteria: a structural view. Microbes and Infection 6, 101-112.
PIZARRO-CERDÁ, J./ COSSART, P. (2006) Bacterial Adhesion and Entry into Host Cells. Cell 124, 715-727.
RAZATOS, A./ ONG, Y.-L. et al. (1998) Molecular determinants of bacterial adhesion monitored by atomic force microscopy. Proc Natl Acad Sci U S A 95, 11059-11064
SEBÉ-PEDRÓS, A./ ROGER, A.J. et al. (2010) Ancient origin of the integrin-mediated adhesion and signaling machinery. PNAS 107(22), 10142-10147.
SOTO, G.E./ HULTGREN, S.J. (1999) Bacterial Adhesins: Common Themes and Variations in Architecture and Assembly. J Bacteriol 181, 1059-1071.
Wissenschaftliche Webseite zur Evolution der Vielzelligkeit:
http://www.broadinstitute.org/annotation/genome/multicellularity_project/MultiHome.html
Autoren: Andreas Beyer / Johannes Sikorski

© AG Evolutionsbiologie des VdBiol. 13.07.2010